陈志杰课题组PNAS:基于四噻吩乙烯的多孔框架复合材料用于增强光催化抗菌活性
细菌、病毒等传染性病原体长期威胁人类健康。以COVID-19为例,其突发性暴发不仅令全球公共卫生体系措手不及,更对经济发展与社会稳定造成深远冲击。临床研究进一步表明,COVID-19患者常伴随继发性细菌感染,且耐药菌株的侵袭显著加剧治疗难度。在此背景下,发展能够高效灭活病原体并阻断其二次或多次传播的新型技术成为迫切需求。光催化抗菌技术因其绿色高效特性,被视为应对高危病原体威胁的理想策略。该技术通过光激发催化剂产生强氧化性活性氧(ROS),在实现微生物高效灭活的同时,兼具低毒副作用的优势。值得注意的是,光催化剂的性能(如ROS生成效率、载流子分离能力等)直接决定抗菌效能。因此,开发兼具高光催化活性与优异生物相容性的功能材料,对推动病原体防控技术的实际应用具有重要价值。
近日,我系陈志杰研究员课题组将光敏性金属有机框架高效整合于可持续基底上,实现功能协同效应,为开发下一代高效抗菌技术开辟了切实可行的路径(图1)。这一研究成果以“Tetrathienylethene-based Porous Framework Composites for Boosting Photocatalytic Antibacterial Activity”为题发表在Proceedings of the National Academy of Sciences of the United States of America(PNAS)上。该论文的第一署名单位为浙江大学化学系,陈志杰研究员为共同通讯作者,化学系博士后马思为本文的第一作者(马思博士即将入职绍兴文理学院)。课题组博士后史乐、杨剑等人共同参与完成该课题。本研究得到了香港理工大学马凯凯助理教授和简志伟教授、香港大学Stoddart教授等多个单位合作完成。本研究得到了国家自然科学基金和浙江省自然科学基金的资助。
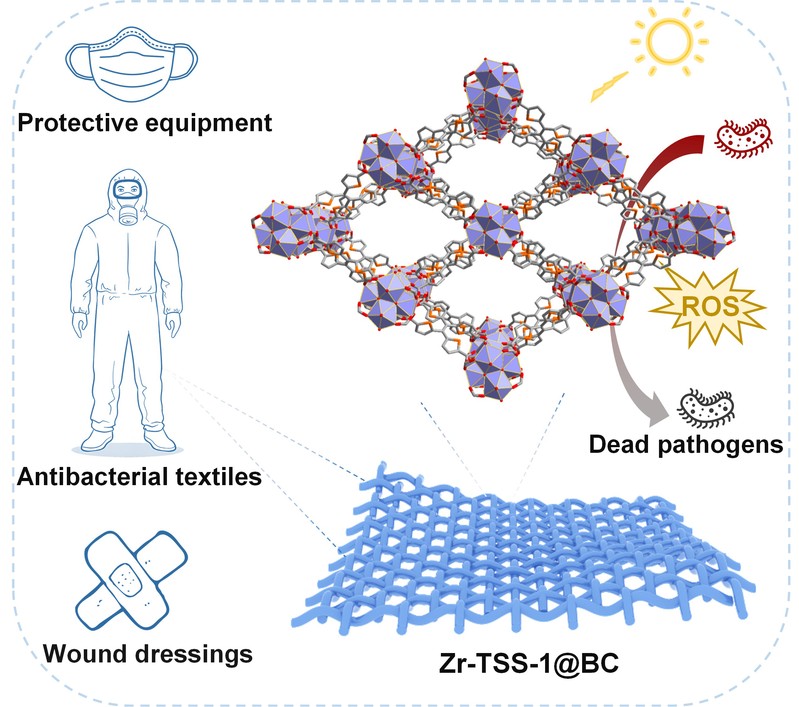
图1. 复合材料的设计示意图及多功能应用场景
相较于大量已报道的四苯乙烯(TPE)基MOFs材料,结构与经典TPE类似的四噻吩乙烯单元(TTE)至今尚未被引入MOF体系。TTE分子中四个具有光敏特性的噻吩基元赋予其优异的可见光响应能力,使其成为构建多孔MOF光催化剂的理想结构单元。基于此,本研究以TTE为核心设计羧酸配体TSS-1:通过CO2与锂化的TTE在无水无氧条件下的反应实现其定向合成。依据网状化学原理与软硬酸碱理论,选择Zr4+作为金属节点,在溶剂热条件下成功制备出Zr-TSS-1单晶。晶体结构解析表明,Zr-TSS-1框架包含两种特征孔道:沿c轴方向可见菱形主通道,而沿b轴观察时,甲酸分子将次级孔道分割为离散空腔(图2)。
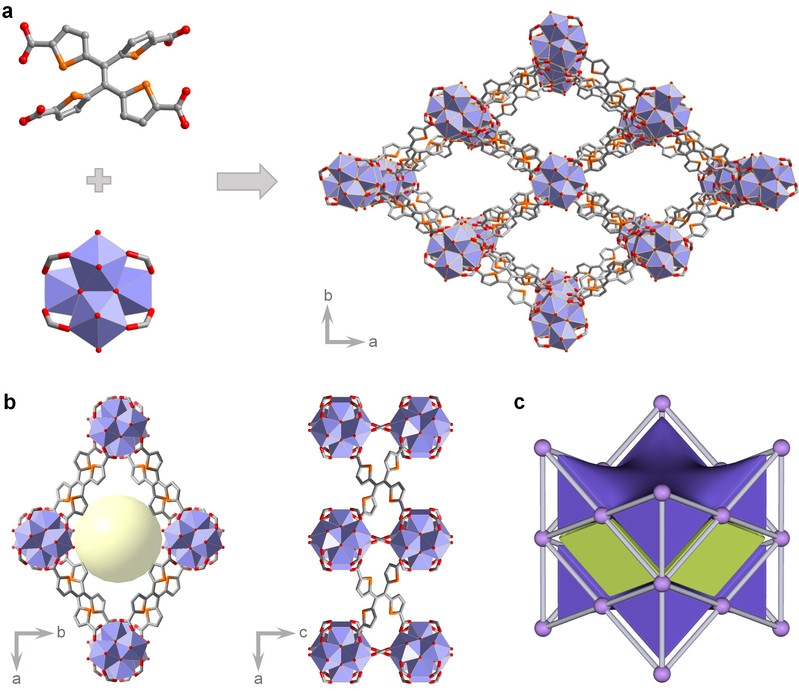
图2. Zr-TSS-1的结构示意图
Zr-TSS-1粉末材料的相纯度通过模拟与实验粉末X射线衍射图谱的高度一致性得以验证。材料表现出优异的孔结构特性:BET比表面积达950 m2 g-1,且在相对压力(P/P0)=0.95时,实验测得总孔容为0.45 cm3 g-1,与理论计算值0.46 cm3 g-1高度吻合。鉴于光催化应用对材料稳定性的严格要求,我们进一步系统评估了Zr-TSS-1的化学稳定性及热稳定性。结果显示:经pH=1~11的酸碱溶液浸泡过夜后,材料仍保持完整的晶体结构;通过变温N2吸附实验证实,其骨架在200 ℃高温下仍保持稳定,表明该材料具备复杂环境应用的潜力(图3)。

图3. Zr-TSS-1的表征
为系统评估材料性能,本研究参照文献方法合成了两种全碳环Zr-MOFs(Zr-TCPE与NU-903),其拓扑结构与Zr-TSS-1类似。紫外-可见漫反射光谱分析表明,Zr-TCPE与NU-903仅在可见光蓝光边缘(~420 nm)呈现窄带吸收,而通过引入四噻吩乙烯单元的Zr-TSS-1展现出显著拓宽的光响应范围(延伸至500 nm)。该现象表明,Zr-TSS-1可实现更高的可见光利用效率与光生激子产率。此外,Zr-TSS-1的光电流密度较对比材料提升3-4倍(图3b),证实其具有更高效的光生电荷分离与迁移能力。能级结构分析表明,Zr-TSS-1的导带位置满足产生活性氧物种·O2-所需电势,而价带位置不足以直接生成·OH。上述结果表明,Zr-TSS-1具备驱动特定光诱导ROS生成的热力学优势,为其作为高效光催化抗菌剂提供了理论依据。
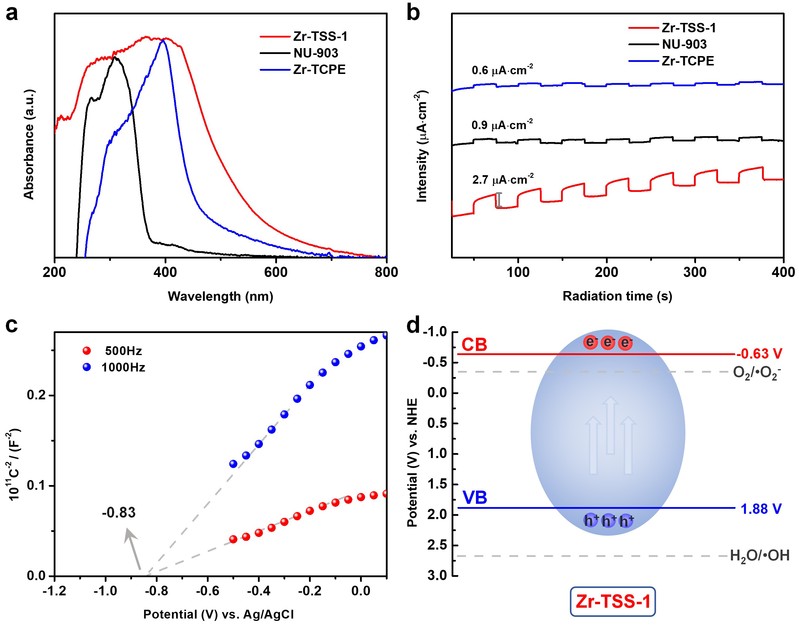
图4. MOFs的光电性能和能级结构
基于细菌纤维素(BC)优异的孔隙率、生物降解性、生物相容性、柔韧性、刚性及耐久性,本研究采用原位生长策略将Zr-TSS-1微晶负载于三维多孔BC骨架(命名为Zr-TSS-1@BC)。PXRD谱图显示复合材料特征峰与原始Zr-TSS-1微晶高度匹配,证实其结构完整性。扫描电镜(SEM)表征表明,Zr-TSS-1微晶在BC基底表面及截面呈规则三维空间分布(图5)。
依据改进版AATCC 100:2019纺织品抗菌测试标准,系统评估了复合材料对革兰氏阴性大肠杆菌(E. coli)与革兰氏阳性金黄色葡萄球菌(S. aureus)的光催化灭活性能。实验采用可见光辐照(光强~4.71 W·m-2),结果显示(图5):Zr-TSS-1@BC在1 h内对两种菌株的灭活率接近100%,而纯BC未表现出显著抑制作用。该抗菌效率显著优于已报道的多数MOF基材料在更高辐照强度下的性能。循环稳定性测试表明,经历五次连续光催化反应后,复合材料的晶体结构仍保持稳定,且对E. coli的抗菌效率未见明显衰减,证实Zr-TSS-1微晶在BC基底中的牢固锚定。
进一步通过细胞毒性实验评估材料生物安全性:与复合材料共培养24小时后,人皮肤细胞及NIH 3T3成纤维细胞的相对存活率均高于~70%(图5),表明Zr-TSS-1对哺乳动物细胞毒性较低。共聚焦显微镜明场图像显示,实验组细胞形态完整,未出现明显损伤;Calcein-AM/PI荧光双染结果显示实验组与对照组活/死细胞比例无显著差异,从分子层面验证了材料的低细胞毒性特性。
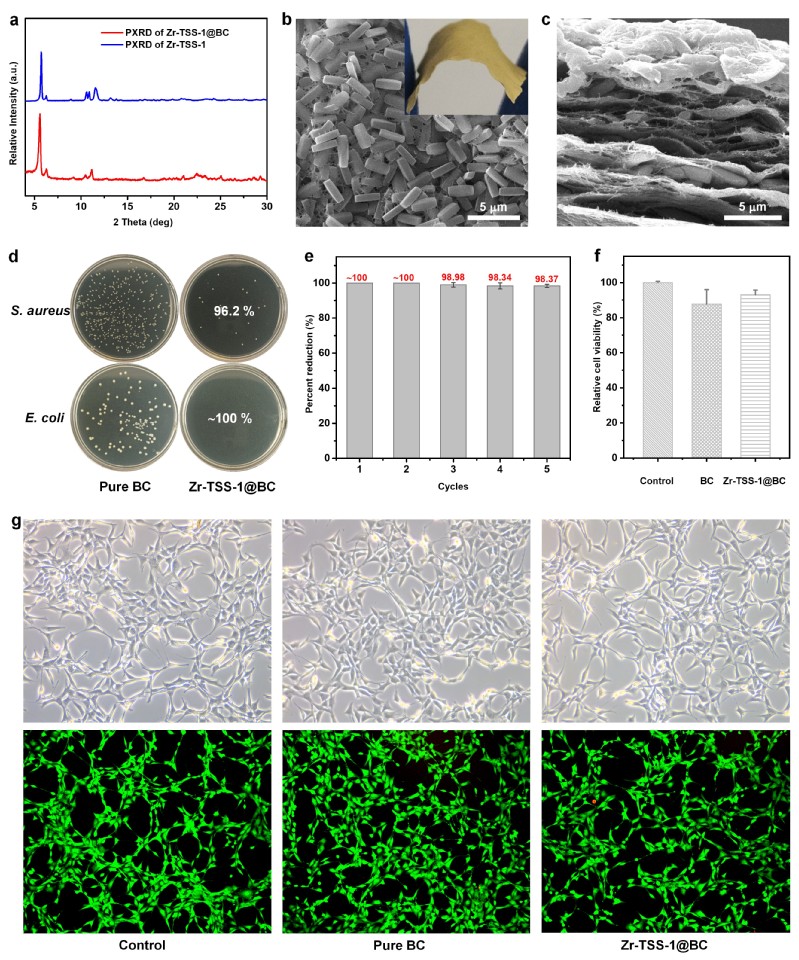
图5. 复合材料的表征及光催化抗菌性能和生物相容性测试
综上所述,本研究通过原位自组装策略,将高稳定性锆基MOF(Zr-TSS-1)与可持续性细菌纤维素(BC)复合,成功构筑了新型光敏复合材料Zr-TSS-1@BC。基于Zr-TSS-1的强可见光捕获能力与优化界面电荷传输动力学,复合材料通过光诱导产生超氧自由基与单线态氧,实现对E. coli及S. aureus近100%的高效灭活。得益于Zr-TSS-1在BC三维多孔网络中的均匀分散及其本征化学/热稳定性,复合材料在连续五次循环使用后仍保持>98%的抗菌效率。细胞毒性实验进一步表明,该材料具有优异的生物相容性。上述特性使Zr-TSS-1@BC在个体防护装备、智能抗菌纺织品及创面敷料等领域展现出广阔应用前景。本研究从分子尺度揭示了生物基复合材料的结构-功能耦合机制,为新一代绿色抗菌材料的理性设计提供了范式参考。
论文详情: S. Ma, Y. Lam, L. Shi, J. Yang, K. Wang, B. Yu, C. Kan, B. Fei, J.H. Xin, K. Ma, J.F. Stoddart, & Z. Chen, Tetrathienylethene-based porous framework composites for boosting photocatalytic antibacterial activity, Proc. Natl. Acad. Sci. U.S.A. 122 (15) e2423052122, https://doi.org/10.1073/pnas.2423052122 (2025).
课题组/导师主页:https://person.zju.edu.cn/zhijiechen#0
文字:陈志杰研究员课题组
编辑:黄珍珍、邹尔纯
审核:林旭锋

