史炳锋教授课题组Angew:钴催化不对称碳氢键活化/插羰环化构建手性异吲哚啉酮
手性异吲哚啉酮是一类重要的手性骨架,广泛存在于天然产物和药物分子中,因此发展手性异吲哚啉酮的高效不对称合成方法,备受关注(图1a)。近年来,过渡金属催化的不对称碳氢键活化为复杂天然产物分子的构筑提供了一种直接、高效的合成策略,为生物活性分子的逆合成分析提供了新的思路。基于不对称碳氢键活化/[4+1]环化反应的两类逆合成分析策略,可实现手性异吲哚啉酮骨架的高效合成(图1b)。Cramer、汪君、李兴伟、游书力和史炳锋课题组先后通过苯甲酰胺与烯烃、炔烃或重氮化合物的对映选择性碳氢键活化/[4+1]环化反应,实现了手性异吲哚啉酮的合成。这些反应操作简单、高效,但需要使用冗长步骤制备的手性配体。考虑到一氧化碳( CO )作为最基本和最容易获得的C1源,苄胺与CO的不对称碳氢键活化/[4+1]插羰环化反应将是一种更有吸引力的合成策略。
浙江大学化学系史炳锋教授团队长期致力于发展绿色高效的廉价金属催化的不对称碳氢键活化新方法,自2019年以来,团队围绕廉价金属钴催化的不对称碳氢键活化,进行了系统而深入的探索。团队发展了大位阻手性酸配体(Chem. Sci.2020, 11, 290; J. Am. Chem. Soc.2021, 143, 19112)和含有氢键受体酰胺基团的联萘/螺环手性酸(J. Am. Chem. Soc.2021, 143, 6810; ACS Catal. 2022, 12, 9806),实现了非手性环戊二烯基钴[CpCo(III)]催化的不对称碳氢键活化。最近,史炳锋教授团队基于对金属钴配位模式的理解,提出了无Cp(cyclopentadienyl,环戊二烯基)配位的正八面体钴催化不对称碳氢键活化新策略,发展了两类新型手性催化体系,实现了廉价金属钴催化的不对称碳氢键活化。2021年,他们率先发展了Co(II)/螺环手性磷酸(SPA)接力催化体系,实现了螺中心手性的构建(Angew. Chem. Int. Ed.2021, 60, 23187)。随后,他们又发展了新型Co(II)/Salox(salicyloxazoline,水杨基噁唑啉)催化体系,以廉价易得的二价钴盐作为催化剂和合成简便且便于改造的Salox手性配体,在体系中原位氧化生成正八面体手性Co(III)催化剂,高效地实现了不对称碳氢键活化/环化反应构建膦中心手性,并成功地分离和表征了相应的正八面体型Co(III)关键反应中间体(Angew. Chem. Int. Ed.2022, 61, e202202892)。随后他们将该催化模式成功应用于双轴手性化合物的构建(Angew. Chem. Int. Ed.2022, 61, e202208912)、膦酰胺不对称碳氢键脱氢烷氧基化和胺化(Angew. Chem. Int. Ed.2022, 61, e202210106; Angew. Chem. Int. Ed.2023, 62, e202302964)及首例对映和区域选择性电氧化钴催化C-H/N-H环化反应(Angew. Chem. Int. Ed.2023, 62, e202218533)、手性二芳基甲胺的构建(Angew. Chem. Int. Ed.2023, 62, e202304706)、联芳轴手性骨架的构建(Angew. Chem. Int. Ed.2023, 62, e202310004)和C1-手性四氢异喹啉(c-THIQs)生物活性分子的不对称合成(J. Am. Chem. Soc. 2023, 145, 24499)。近日,该团队成功地将Co(II)/Salox催化体系拓展应用于手性异吲哚啉酮骨架的不对称碳氢键活化/[4+1]插羰环化反应中,相关成果近期在线发表于Angew. Chem. Int. Ed.上。
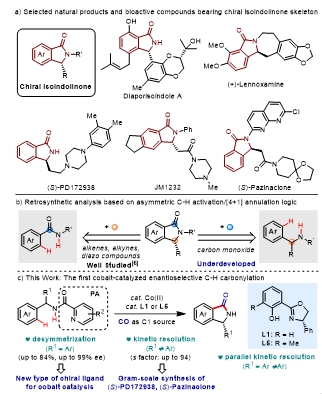
图1. Co(II)/Salox催化不对称碳氢键活化/[4+1]插羰环化反应。图片来源:Angew. Chem. Int. Ed.
受先前研究成果的启发,作者设想将Co(II)/Salox催化体系应用于二芳基甲胺类化合物的不对称碳氢键插羰环化反应,实现手性异吲哚啉酮骨架的构建。然而,面临的挑战有:1)CO作为σ-给体/π-受体的强配位能力会与手性配体产生强烈的竞争;2) CO气氛下金属离子发生还原会导致催化剂失活;3) 缺乏合适的配体实现高效的反应活性和对映选择性控制。鉴于此,作者发展了Co(II)/Salox催化不对称碳氢键/[4+1]插羰环化反应,以CO作为C1源,实现了手性异吲哚酮化合物的构建,并通过生物活性化合物(S)-PD172938和(S)-Pazinaclone的不对称全合成,证明了该方法的合成潜力。同时,所得到的手性异吲哚啉酮化合物也可作为手性配体参与钴催化不对称碳氢键活化/插炔环化反应,构建膦中心手性(图1c)。
首先,作者以α-苯基吡啶甲酰胺1aa作为模型底物,在CO气氛下,进行了相关反应条件筛选。在最优条件下可以以27 %的收率和94 %的对映选择性得到脱保护的异吲哚啉酮产物2a,吡啶甲酸导向基可作为无痕导向基原位脱除。考虑到导向基的可拆卸性和Salox配体与移除的吡啶甲酸导向基之间的配位竞争,作者随后考察了不同取代吡啶甲酸导向基,结果表明以3-甲基吡啶甲酸合成的α-苯基吡啶甲酰胺1a为起始原料,用Zn/1.5 M HCl处理粗品,原位一锅法除去导向基后,可以以51 %的收率和95 %的对映选择性得到产物2a。作者通过后续的相关反应条件筛选,得到的最优反应条件是:草酸钴(10 mol%)作为催化剂,(S)-L5(15 mol%)作为配体,CsOAc(1.5 equiv)作为添加剂,AgNO3(2.0 equiv)作为氧化剂,在1,4-dioxane(0.2 M)溶剂中100 ℃反应24小时后,可以79%的收率、98%的对映选择性得到产物2a。
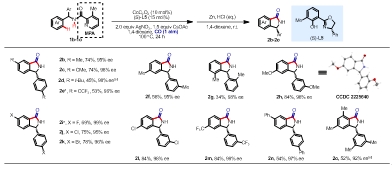
图2. α-芳基吡啶甲酰胺底物范围。图片来源:Angew. Chem. Int. Ed.
在获得上述最佳反应条件后,作者对α-芳基吡啶甲酰胺底物1的范围进行了考察(图2)。各类含供电子基、吸电子基的α-芳基吡啶甲酰胺底物均能有效兼容(2b-2e & 2i-2k, 45-78%, 95-99% ee)。随后,作者通过X射线衍射分析确定了2h的绝对构型,其他产物的立体构型可类比得知。作者还展示了Co(II)/Salox催化的含有两个不同芳香基团的外消旋α-取代苄酰胺底物的平行动力学拆分过程(图3) 。
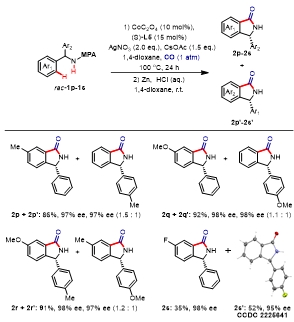
图3.平行动力学拆分底物范围。图片来源:Angew. Chem. Int. Ed.
此外,该Co(II)/Salox反应体系还能实现外消旋α-取代苄酰胺底物的动力学拆分(图4)。在优化吡啶甲酸导向基后,对反应条件进行调整后,得到最优反应条件。各种外消旋保护的氨基醇和氨基酸衍生物都具有良好的底物兼容性,获得了良好至优异对映选择性的环化产物2和手性氨基醇或氨基酸衍生物1(2t-u , 89-93% ee ; 1t-u , 86-93% ee)。以天然分子麝香草酚和手性药物布洛芬为核心结构衍生的更复杂的底物也具有很高的反应效率。
随后,为了展示Co(II)/Salox催化不对称C-H/[4+1]插羰环化反应的合成应用潜力,作者以(R)-L1为手性配体对外消旋苄酰胺底物1t进行动力学拆分,原位一步脱除TFA导向基及TBS保护基,得到关键的手性异吲哚啉酮(S)-3药物前体,后续经亲核取代、氧化、Buchwald-Hartwig偶联等步骤,实现了生物活性化合物(S)-PD172938和(S)-Pazinaclone的不对称全合成(图4)。
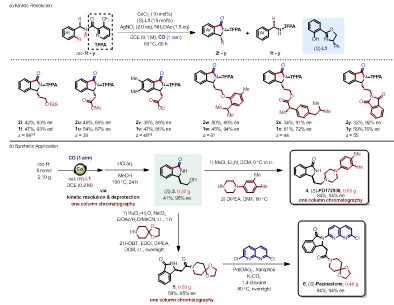
图4. 合成应用。图片来源:Angew. Chem. Int. Ed.
手性γ -内酰胺是一类在不对称催化中被广泛应用且易于获得的手性配体/有机催化剂。然而,这些手性配体和催化剂的优势骨架很大程度上依赖于L-焦谷氨酸的衍生。作者认为手性异吲哚啉酮类化合物可以作为γ -内酰胺分子的类似物,并且苯环的空间和电子性质的微调可能为配体的设计和应用带来启发(图5a)。
作者在对Co(II)催化不对称碳氢键活化的手性配体的初步研究中发现,使用L-焦谷氨酸甲酯作为手性配体,在对Co(II)催化芳基膦酰胺7与二苯基乙炔8的不对称碳氢键活化/插炔环化反应中,可以以15%的产率和21%的对映选择性得到环化产物9(图5b)。当使用手性异吲哚啉酮(R)-2a时,环化产物9的反应活性和对映控制选择性略有增加。通过调节电子效应,当(R)-2i用作配体时,可以以89%的收率和82%的对映选择性得到环化产物9。作者猜测可能是因为底物与配体之前存在的π-π堆积作用使得反应诱导出良好的对映选择性,同时氟原子的引入可能增强了酰胺的去质子化能力,并有助于提高与钴中心的配位强度。
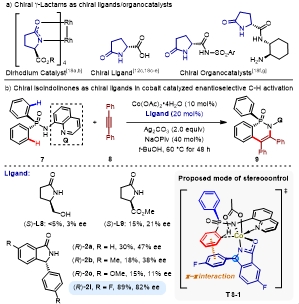
图5. 催化应用。图片来源:Angew. Chem. Int. Ed.
综上,浙江大学化学系史炳锋教授团队报道了Co(II)/Salox催化的不对称碳氢键活化/[4+1]插羰环化反应。该反应体系以廉价易得的钴盐作为催化剂、易制备的水杨基噁唑啉作为手性配体,条件温和、立体选择性高,为手性异吲哚啉酮骨架的高效绿色合成提供了新的方法。生物活性化合物的不对称全合成如(S)-PD172938和(S)-Pazinaclone证明了该策略的潜在合成应用价值。此外,在Co(II)催化的不对称碳氢键活化反应中,手性异吲哚啉酮可被用作一种新型的手性配体。
该论文的通讯作者是浙江大学史炳锋教授和百人研究员姚启钧,第一作者是2020级直博生滕茗芽,吴勇杰等同学共同参与完成该课题。
Cobalt-Catalyzed Enantioselective C−H Carbonylation towards Chiral Isoindolinones
Ming-Ya Teng, Yong-Jie Wu, Jia-Hao Chen,[a] Fan-Rui Huang, De-Yang Liu, Qi-Jun Yao,* and Bing-Feng Shi*
Angew. Chem. Int. Ed.2023, DOI: 10.1002/anie.202318803
导师介绍https://person.zju.edu.cn/bfshi
文 字:史炳锋教授课题组
编 辑:黄珍珍、张维娅
审 核:林旭锋

