苏彬课题组Angew:T细胞肿瘤抗原识别的电化学发光成像
T细胞表位抗原疫苗与T细胞受体(TCR)-T细胞疗法是抗肿瘤领域两种新颖的免疫治疗策略,显示出极为优越的疗效。T细胞表位抗原疫苗是通过引入特定肿瘤抗原多肽,刺激患者体内自身T细胞产生高效肿瘤免疫应答;而TCR-T细胞疗法则利用基因工程技术使T细胞表达特定肿瘤特异性TCR克隆,高效识别肿瘤抗原并杀死肿瘤细胞。准确筛选并鉴定有效肿瘤特异性抗原多肽及TCR克隆是肿瘤治疗领域的一大难点。
近日,苏彬课题组通过免疫突触的电化学发光(ECL)成像,实现了T细胞肿瘤抗原识别的免标记分析(图1)。将特异性刺激分子修饰在基底电极表面,刺激并激活T细胞,使其形成免疫突触。由于细胞粘附抑制ECL反应,因此ECL图像中免疫突触形成区域表现为暗斑。通过分析细胞的铺展面积和识别强度来评估免疫突触的结合特性,实现了对不同种类肿瘤抗原(pMHC)、不同抗原反应性的TCR以及形成免疫突触所需的相关辅助分子(如信号传递分子CD3、共刺激分子CD28和粘附分子LFA1)的区分。这种免标记的成像策略有望应用于高效肿瘤特异性抗原多肽及TCR克隆的筛选与鉴定。相关成果最近发表在德国应用化学期刊上(Angew. Chem. Int. Ed. doi.org/10.1002/anie.202314588)。
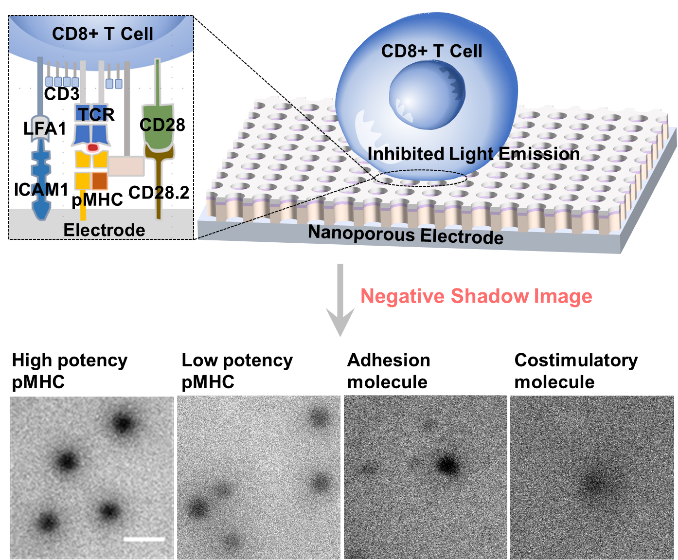
图1. T细胞抗原识别和区分的免标记ECL成像示意图
T细胞通过其表面的TCR识别肿瘤细胞上的特异性抗原,与肿瘤细胞形成稳定免疫突触,从而释放穿孔蛋白酶和细胞因子等,以达到杀伤肿瘤细胞的目的。鉴于免疫突触结构决定着T细胞对肿瘤细胞的杀伤,可将其作为T细胞肿瘤特异性抗原识别的特征。目前,通常运用荧光成像技术(如全内反射荧光成像)来表征免疫突触的形成。但其需要额外的荧光标记,且易受细胞自体荧光和荧光分子光漂白特性的限制。因此,迫切需要开发快速和免标记的成像方法来表征免疫突触的形成,用于鉴定有效的肿瘤特异性抗原多肽及TCR克隆。
课题组前期工作采用ECL成像技术实现了对细胞黏着和细胞间连接的顺次成像。在此基础上,该工作通过改变ECL分子与共反应剂的浓度比来调控ECL反应路径,以获得限域或延展的发光层(分别对应氧化还原路径和催化路径),并将其应用于T细胞免疫突触成像。实验结果表明氧化还原路径主导的电化学发光更适合成像免疫突触(图2)。这是因为免疫突触是在T细胞基底膜与电极表面接触的微区内形成,表面限域的发光层才能有效地对免疫突触这一界面结构进行良好观察。

图2. 调控发光层厚度,成像T细胞免疫突触
随后采用上述表面限域ECL成像体系对多种肿瘤抗原多肽及不同克隆TCR-T细胞进行配对识别验证。结果显示,ECL可对TCR-T细胞与对应的特异性肿瘤抗原形成稳定的免疫突触结构进行成像;通过对ECL图像进行分析,定量评估免疫突触形成的面积和强度,实现了T细胞抗原识别强弱的区分(图3)。
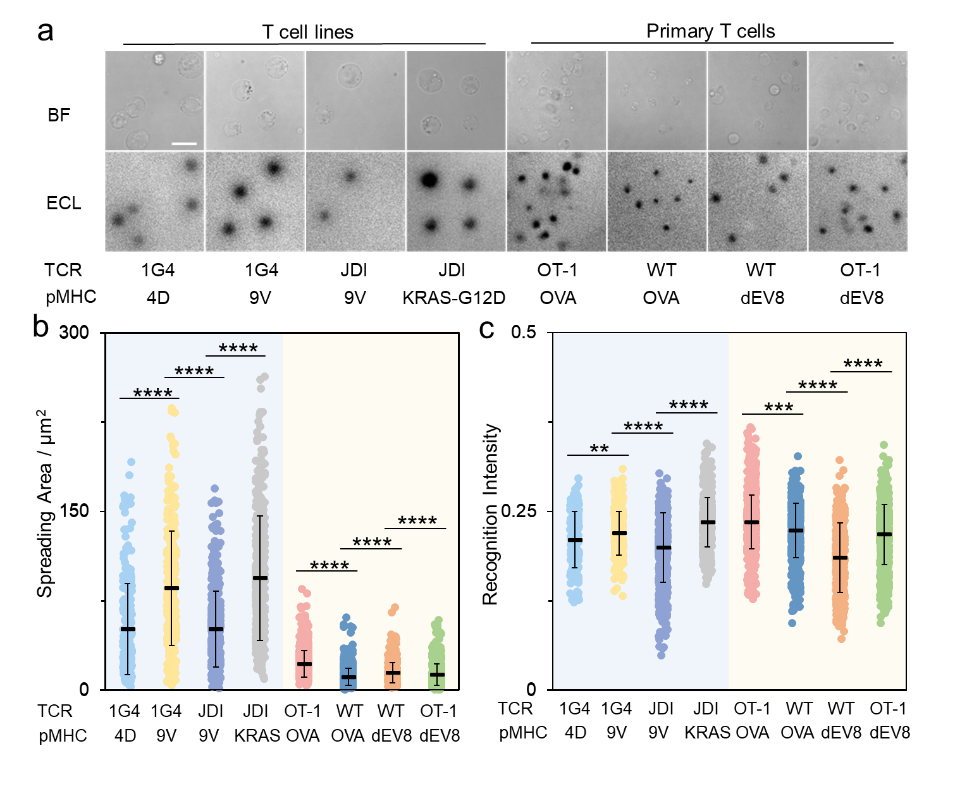
图3. 对多种肿瘤抗原多肽及不同克隆TCR-T细胞进行配对识别验证
综上所述,该工作开发了一种T细胞免疫突触的免标记ECL成像技术,并将其用于肿瘤特异性抗原多肽及TCR克隆的鉴定。该技术有望用于肿瘤特异性抗原及TCR克隆的筛选,这对T细胞表位抗原疫苗与TCR-T细胞疗法的发展至关重要。
本文的作者是浙江大学化学系博士研究生颜亚娟(化学系21级直博生)、浙江大学生物系统工程与食品科学学院博士后周萍和浙江大学化学系博士研究生丁鹭榕(化学系23级硕博连读生)。通讯作者是浙江大学化学系苏彬教授、基础医学院陈伟教授和医学院附属第一医院胡炜特聘研究员。该项目受到国家自然科学基金的经费资助。
文章链接:https://doi.org/10.1002/anie.202314588
课题组链接:https://mypage.zju.edu.cn/binsu/696525.html
文 字:苏彬教授课题组
编 辑:张维娅
审 核:黄珍珍、林旭锋
终 审:丁立仲

