陆展课题组Nature Communication: 阴离子型三氮配体促进钴催化支链选择性合成1,4-二烯
1,4-二烯是一类重要的结构片段,存在于多种类型的生物活性天然产物中。例如,间链胞霉酸是一种包含1,4-二烯片段的真菌萌发抑制剂。利泊汀及、前沟藻内脂、默诺醇等也都是包含1,4-二烯片段的抗菌活性药物分子。除此之外,众多不饱和脂肪酸中也含有1,4-二烯片段,例如花生四烯酸是人体所必须的脂肪酸。然而,在目前已有的合成方法中,往往需要使用当量的金属试剂介导烯烃或者炔烃C-C键偶联,进而合成相应的1,4-二烯化合物(图1a)。
过渡金属氢催化剂催化炔烃的氢烯丙基化反应能够直接高效的构建新的碳碳键以及新的碳氢键,引入一个烯丙基片段,避免当量金属试剂的使用,是一种理想用于合成1,4二烯的强有力方法。末端炔烃选择性的插入到金属氢键中,得到烯基金属中间体,再与亲电试剂发生反应,进而得到功能化的烯烃化合物。然而,通过金属氢催化的策略实现选择性氢烯丙基化反应仍具有很大的挑战性:(1) 由于原位生成的烯基金属中间体具有较高的反应活性和不稳定性,与反应体系中的其他试剂存在兼容性问题。例如,在反应过程中与金属氢化物发生配体交换、炔烃的金属碳化,进而影响反应的化学选择性。(2) 相比于未活化的烷基亲电试剂与烯基金属中间体的直接偶联,活化的烯丙基亲电试剂更容易与其他亲核试剂发生多种副反应。例如,烯丙基溴会与原位生成的金属氢活性中间体发生脱卤氢化反应。(3) 由于末端炔烃较弱的电子和空间效应,金属氢键更倾向于进行反马氏类型的插入而不是马氏类型插入(图1b)。目前,使用金属氢物种催化炔烃选择性亲电氢烯丙基化反应仅有有限的报导例子。2017年,Lalic课题组应用大位阻的氮杂环卡宾铜氢催化剂实现了末端炔烃的反马氏氢烯丙基化反应(J. Am. Chem. Soc.2017, 139, 6969-6977)。然而,对于金属氢催化炔烃的马氏选择性亲电氢烯丙基化反应目前还未有报道的例子(图1c)。
浙江大学化学系陆展课题组从2012年底建组以来一直致力于设计与合成适用于铁、钴等地球丰产过渡金属的三齿含氮配体(Acc. Chem. Res.2021, 54, 2701),并成功将其应用于铁或钴催化不饱和烃类化合物的高选择性氢官能团化反应中,例如: 硼氢化 (Org. Lett. 2014, 16, 6452; Nat. Commun. 2018, 9, 3939; J. Am. Chem. Soc.2017, 139, 15316)、 硅氢化 (Angew. Chem. Int. Ed. 2015, 54, 4661; J. Am. Chem. Soc. 2017, 139, 9439)、氢化 (Org. Lett. 2016, 18, 1594; J. Am. Chem. Soc. 2021, 143, 12433)、氢胺化 (Nat. Commun.2020, 11, 783)等反应。2016年,该课题组独立设计和发展了一类新型的NNN-三齿阴离子配体(Org. Lett.2016, 18, 4658;)。这种类型的配体具有类平面、小空腔的特点,具有可控修饰位点多、容易大规模合成的优点,并与原子半径小、较强路易斯酸的铁、钴等过渡金属展现出良好的兼容性(Org. Lett. 2017, 19, 969–971;ACS Catal. 2019, 9, 4025; Nat. Commun. 2022, 13, 650)。该类型的配体能够用于促进金属钴催化炔烃的高选择性转化(J. Am. Chem. Soc.2020, 142, 14455; Angew. Chem., Int. Ed. 2021, 60, 690)。基于该研究体系,陆展课题组首次实现了金属钴催化末端炔烃的马氏选择性氢烯丙基化反应,高效、高选择性地合成了高附加值的1,4-二烯化合物 (图1d)。相关成果最近发表在自然-通讯期刊上 (Nat. Commun.2022, 13, 4518)。
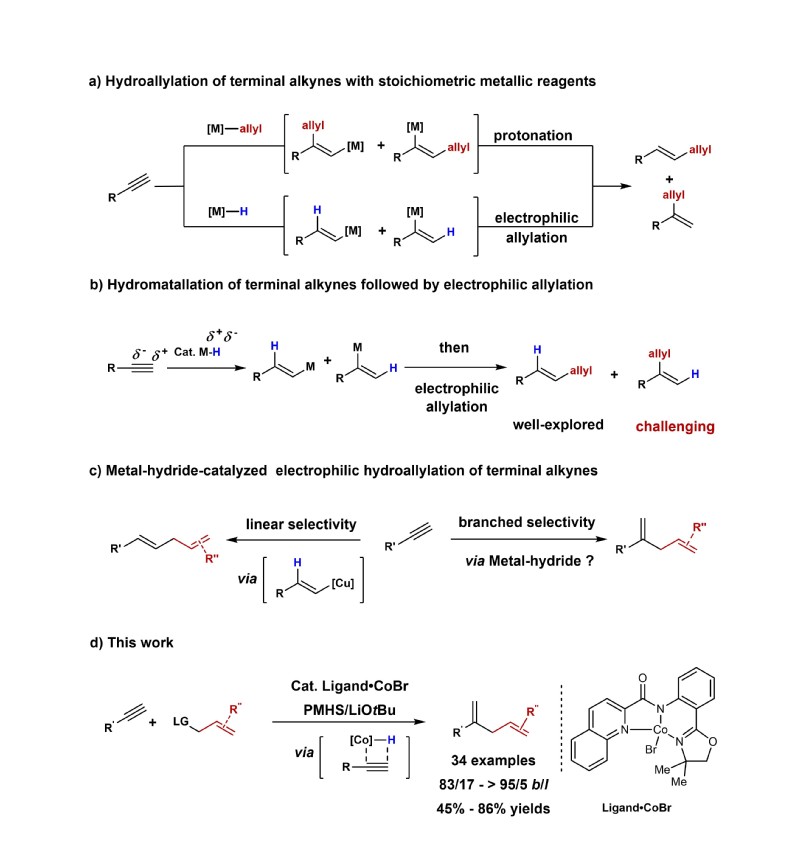
图1. 末端炔烃的氢烯丙基化反应
结果与讨论:
由于阴离子三齿配体(喹啉酰胺苯基噁唑啉)能够用于金属钴催化炔烃的氢官能团化过程中的选择性调控,并且在反应中表现出良好的区域选择性调控效果。因此,作者首先使用阴离子三齿配体喹啉酰胺苯基噁唑啉以及醋酸钴作为预催化剂,烯丙基溴作为亲电试剂,叔丁醇锂作为金属醇盐,聚甲基氢硅氧烷作为氢源,来探究在该体系下是否能发生炔烃的氢烯丙基化反应。在条件筛选过程中,作者发现阴离子三齿含氮配体(L1-L8)中取代基对反应的选择性会产生显著的影响(图2)。
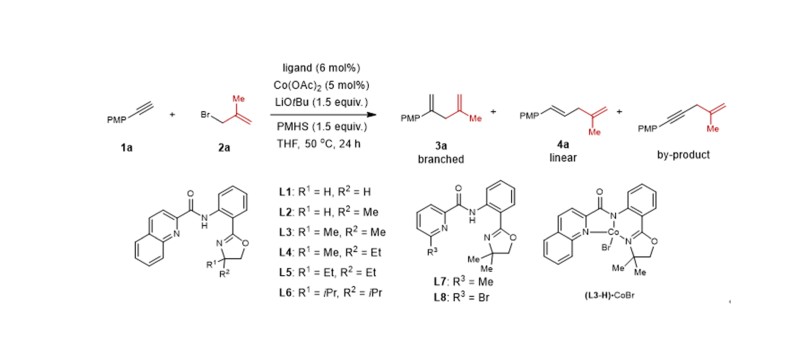
Entrya | Variations from “standard conditions” | Yield of 3/4 (%)b | α/βb |
1 | L1 | 42 | 83/17 |
2 | L2 | 40 | 89/11 |
3 | L3 | 70 | >95/5 |
4 | L4 | 55 | 94/6 |
5 | L5 | 45 | 91/9 |
6 | L6 | 70 | 85/15 |
7 | L7 | 83 | 91/9 |
8 | L8 | 53 | 92/8 |
9 | (L3-H)•CoBr; 1 h | 75 (69) | >95/5 |
图2. 氢烯丙基化反应条件筛选
该反应具有广阔的底物范围,良好的官能团容忍性,反应条件温和,适用于多种末端炔烃的转化。为了验证反应的底物的普适性,作者也对不同的烯丙基亲电试剂进行考察。除了烯丙基溴之外,其他亲电试剂,例如烯丙基碘、苄基溴在该反应体系下也能够兼容。为了能够体现该反应的实用性,作者也进行了克级规模的放大,多种产物能够扩大到克级规模生产,并且能够通过简单的蒸馏得到相应的产物,具有潜在的应用价值(图3)。
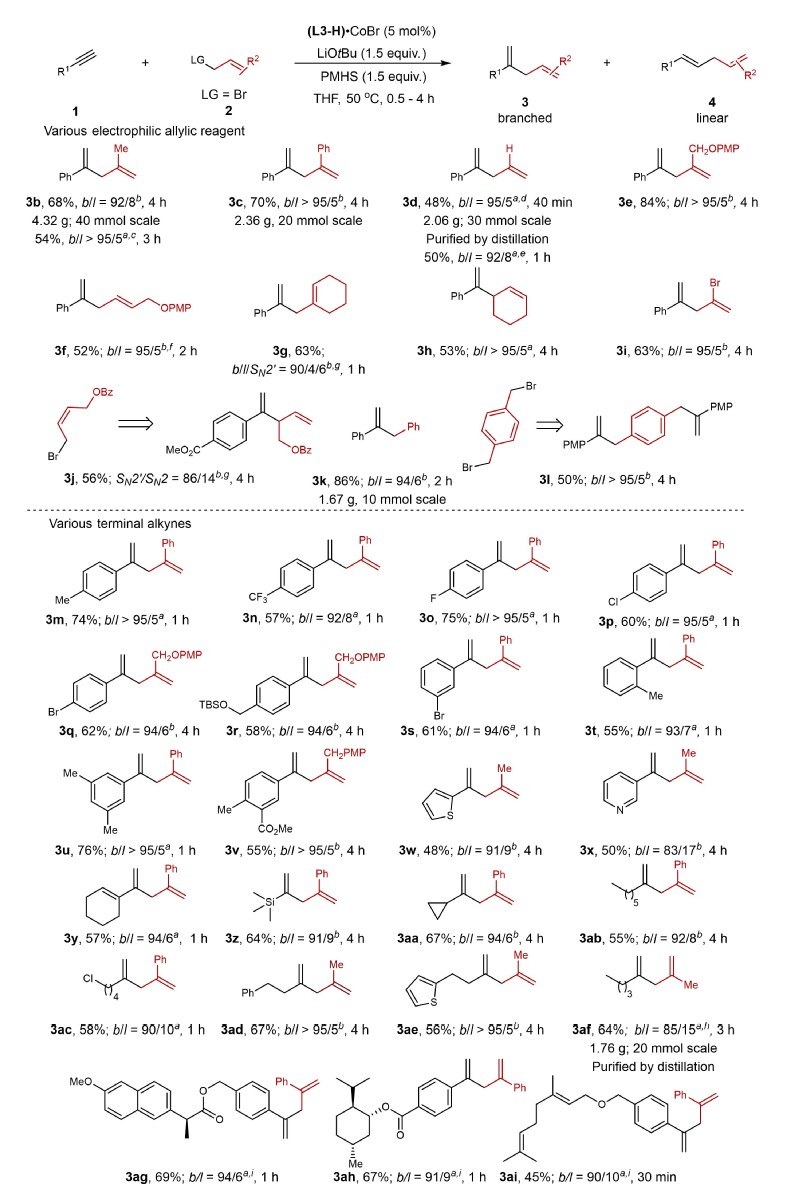
图3. 氢烯丙基化反应底物范围
在该氢烯丙化反应中,催化剂的催化循环次数可以高达1160次。说明在该反应过程中,催化剂具有极高的稳定性。并且1,4-二烯化合物也可以发生多种多样的转化。例如,两个烯烃双键可以选择性发生两次硅氢化生成硅杂环或者二硅化合物,烯烃的两个双键可以选择性转化其中的一个双键制备高附加值化合物(图4)。
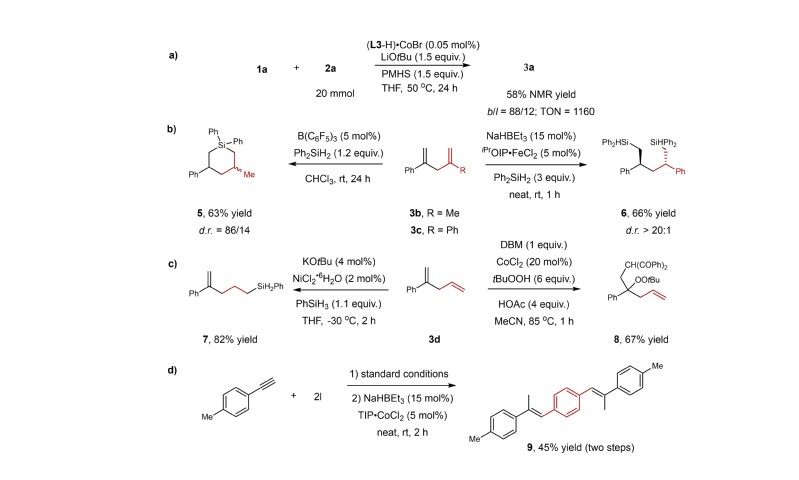
图4. 1,4-二烯化合物的衍生化转化
最后,作者结合先前的报导研究以及根据相应的机理实验,提出了一种可能的机理:活性中间体(L3-H)•CoBr与LiOtBu、硅烷反应得到活性金属钴氢物种C。末端炔烃与活性物种C配位,然后末端炔烃插入到金属钴氢键中,从而产生占主导的α-选择性的烯基金属钴中间体E。E和钴卡宾两性离子F之间的快速异构化平衡导致氘代底物氢烯丙基化过程中E/Z比发生改变。活性中间体E与烯丙基亲电试剂经历SN2'或者SN2类型的亲电取代反应,进而得到相应的二烯化合物。在该催化过程中,合适的配体选择以及硅烷和醇盐会对产物的选择性改变产生影响。
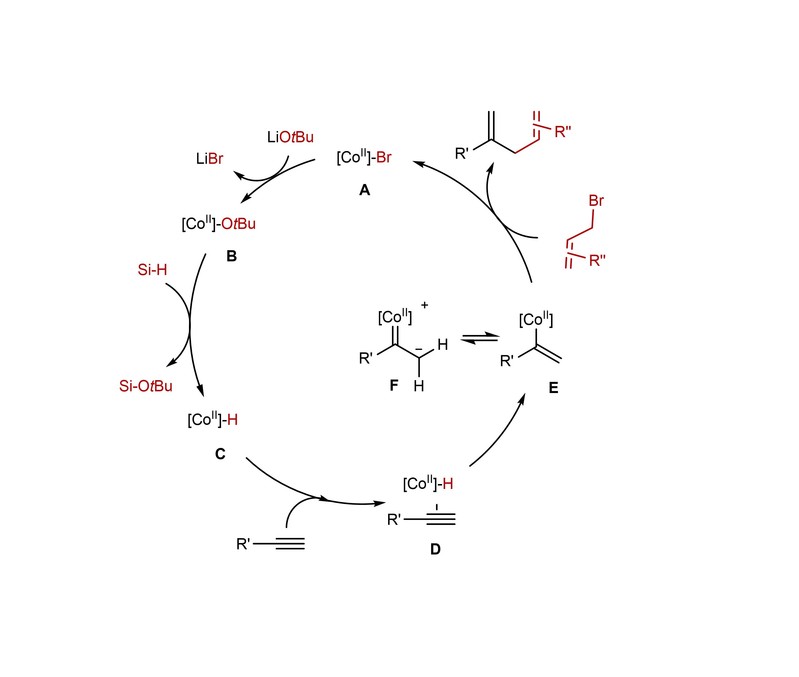
图5. 可能的反应机理
小结:
浙江大学陆展课题组利用配体调控金属氢催化的策略,首次实现了金属钴氢催化末端炔烃高马氏选择性氢烯丙基化反应,高效高选择性地制备了高附加值的1,4-二烯化合物。在该反应中,作者实现了挑战性的末端炔烃以马氏选择性为主导的插入到金属氢键中;成功制备了活性钴溴中间体,为相关活性物种的制备提供了借鉴意义;解决了反应过程中,高活性的金属氢物种、烯基金属物种与高活性的亲电试剂的兼容性问题。在该反应中,理性的配体设计对于反应的区域选择性调控起着至关重要的作用。基于该类型的配体设计,作者希望将相关的配体应用到炔烃的区域选择性氢官能团化反应中,发展多样性的氢官能团化反应,并为炔烃氢官能团化过程中的区域选择性调控机制研究提供借鉴意义。
本文第一作者是浙江大学化学系博士研究生陈杰坪(化学系18级硕博连读生),本文第二作者为化学系21级硕士生应佳乐,通讯作者是陆展教授。该项目受到国家自然科学基金优青项目和面上项目、浙江省自然科学杰出青年基金、浙江大学化学前瞻技术中心、科技部催化专项、科技部基础科研条件与重大科学仪器设备研发重点专项等经费资助。同时,感谢浙江大学争创优秀博士学位论文项目对博士研究生陈杰坪的资助。
原文链接:https://www.nature.com/articles/s41467-022-32291-3
陆展研究员个人主页:https://person.zju.edu.cn/lu/

