史炳锋课题组:Pd(II)催化硫醚导向不对称烯烃碳氢键活化构建具有共轭二烯结构的手性苯乙烯
烯烃作为一类重要的合成子,广泛存在于天然产物、药物和材料分子中。一个烯烃分子拥有四个取代位点,可以被不同的取代基取代,同时烯烃的E/Z异构化也有效地增加了烯烃结构的多样性。而且当连接取代烯烃和芳烃的碳碳单键旋转受阻时,又会产生一对阻转异构体。这些都使得立体选择性地合成多取代烯烃变得更加的复杂和具有挑战性(Scheme 1a)。
在过去几十年中,手性烯烃作为配体在不对称合成中取得了可喜的应用。这些手性烯烃结构主要包括基于手性碳骨架的手性双烯或含杂原子辅助配位的烯烃配体和基于手性硫原子中心的手性硫烯配体两类。受到近期手性苯乙烯合成和应用迅速发展的启发,史炳锋课题组设想结合轴手性和硫中心手性的烯烃物种是否可以为手性烯烃的应用增加新的可能性(Scheme 1b)。但是相比于联芳轴手性化合物,烯烃轴手性化合物因为其比较低的翻转能垒,使得对其手性构建更具挑战的。迄今为止,催化不对称构建手性苯乙烯骨架的策略主要有两种:(1)由Tan、Yan和Shi课题组发展的有机小分子催化策略;(2)由史炳锋课题组和Wang课题组发展的不对称芳烃碳氢键官能团化策略(Scheme 1c)。虽然这些方法可以很好的构建含有非环结构的手性苯乙烯轴手性化合物,但是立体选择性的构建具有多取代的共轭1,3-二烯结构的手性苯乙烯迄今尚未实现。
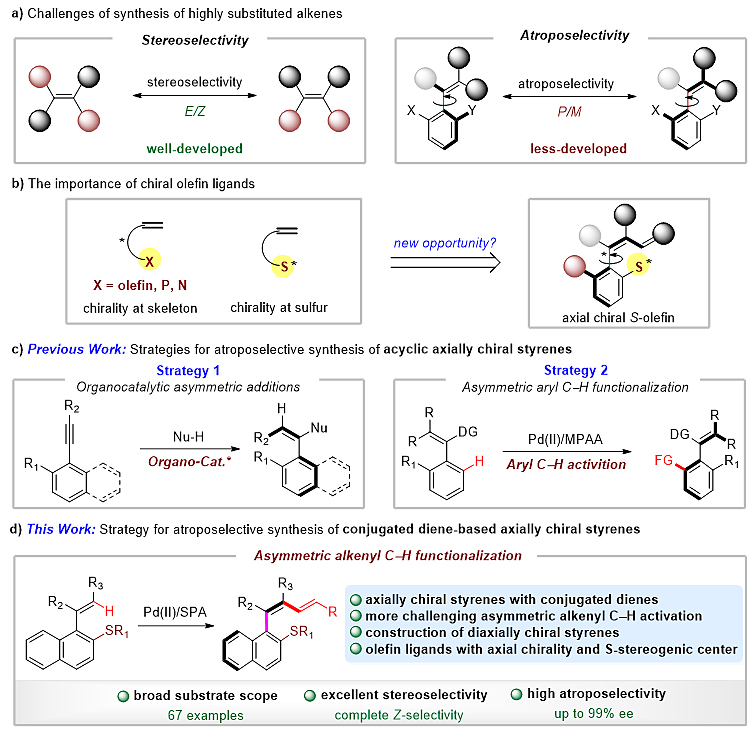
Scheme 1. Challenges and Strategies for the Construction of Atropisomeric Styrenes with a Conjugated Diene Moiety
近年来,史炳锋课题组在不对称碳氢键活化构建轴手性方面开展了系统性的研究:
1)基于“瞬态手性辅基”策略,以商业上廉价易得的叔亮氨酸(Tle)为手性有机小分子催化剂,实现了轴手性联芳基醛化合物的高效和高对映选择性合成(Angew. Chem. Int. Ed., 2017, 56, 6617; Angew. Chem. Int. Ed., 2018, 57, 3661; Angew. Chem. Int. Ed., 2018, 57, 17151; ACS Catal., 2019, 9, 1956; Org. Lett., 2019, 21, 3352; Organometallics, 2019, 38, 4022; Angew. Chem. Int. Ed., 2019, 58, 11464; Angew. Chem. Int. Ed., 2020, 59, 6576; CCS Chem., 2021, 3, 455。综述:Chem. Commun., 2019, 55, 8514; Angew. Chem. Int. Ed., 2020, 59, 19773; Chin. J. Org. Chem., 2020, 40, 3517)。
2)发展Pd(II)/手性螺环磷酸(SPA)催化体系构建联芳基轴手性化合物 (Angew. Chem. Int. Ed., 2019, 58, 6708; Angew. Chem. Int. Ed., 2020, 59, 3568; Org. Lett., 2020, 22, 9693)。
3)发展Pd(II)/焦谷氨酸(L-pGlu)催化体系构建烯烃轴手性骨架(Chem, 2020, 6, 497)和酰胺轴手性骨架(J. Am. Chem. Soc., 2020, 142, 18266; Chem. Sci., 2021, 12, 9391)。
最近,该课题组利用Pd(II)/手性螺环磷酸催化体系,通过不对称烯烃碳氢键烯基化反应,实现了具有多取代1,3-共轭二烯结构的手性苯乙烯的不对称构建(Scheme 1d)。该反应底物范围广泛且具有优秀的产率、高对映选择性和完全的顺式选择性。
研究人员首先以带有硫醚为导向基的苯乙烯1a为模板底物,丙烯酸酯2a为烯基化试剂,对反应的溶剂、温度和手性配体进行了筛选(Table 1)。最终发现当使用3,3’-具有大位阻取代的SPA L11作为手性配体,乙醚为溶剂,醋酸钯为催化剂时,可以以94% yield和95% ee,完全的顺式选择性得到目标的烯基化产物3aa。
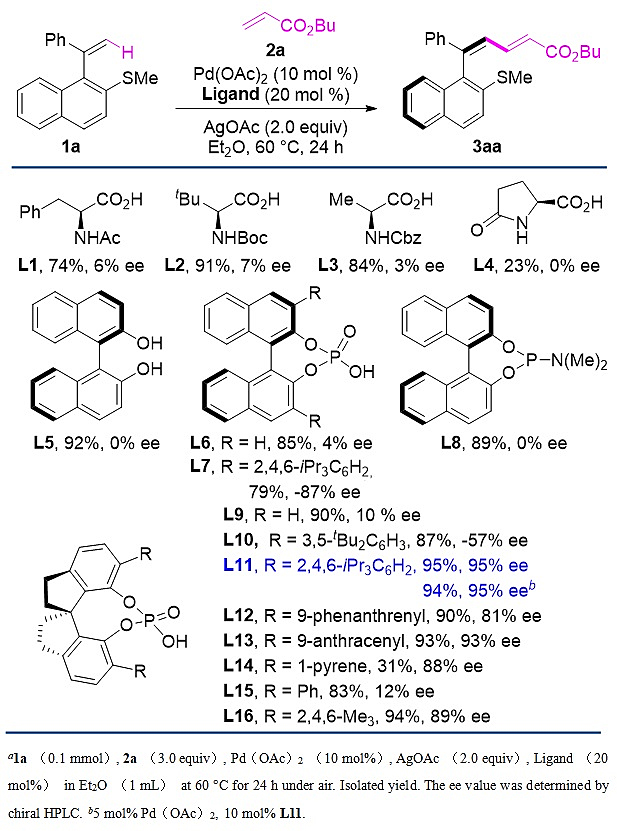
Table 1. Optimization of C-H Olefinationα
在最优反应条件下,不同位阻大小的硫醚导向基(Table 2a),不同芳基取代的苯乙烯底物(Table 2b),以及不同烷基链取代的苯乙烯底物(Table 2c)均可以以优秀的产率和对映选择性得到三取代的共轭二烯结构的手性苯乙烯化合物。
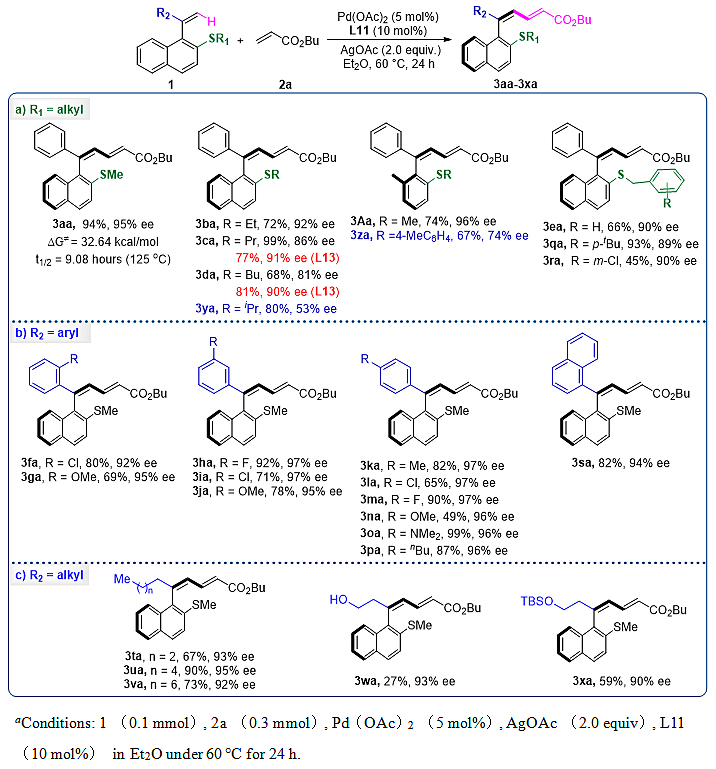
Table 2. Scope of Pd(II)-Catalyzed Atroposelective C‒H Olefination for the Synthesis of Trisubstituted Alkenes.α
随后研究人员考察了四取代的1,3-共轭二烯结构的手性苯乙烯化合物的合成普适性(Table 3)。反应可以在额外增加当量的金刚烷甲酸的作用下得到中等以上产率和优秀的对映选择性。
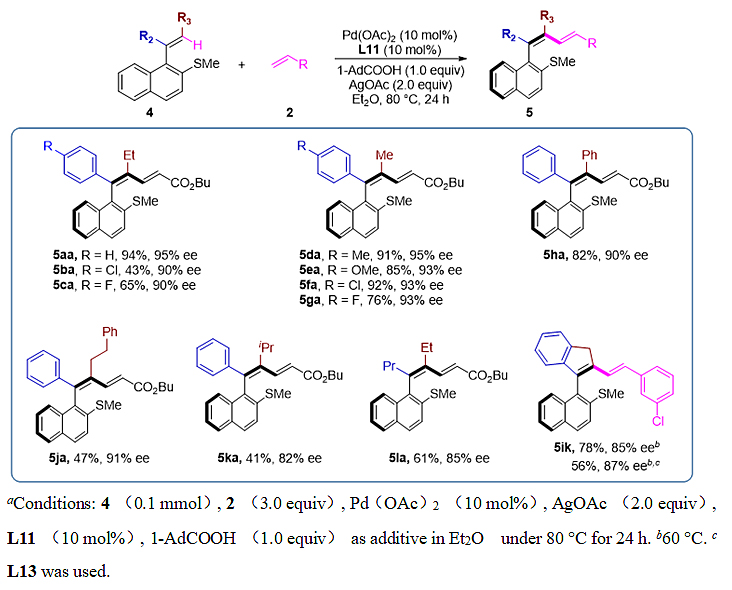
Table 3. Scope of Pd(II)-Catalyzed Atroposelective C-H Olefination for the Synthesis of Tetrasubstituted Alkenes. α
之后研究人员对反应的烯基化试剂进行了拓展。发现不同取代基的丙烯酸酯和苯乙烯均可以作为该反应有效的烯基化试剂。同时,许多天然产物和活性分子衍生的烯基化试剂也可以在最优条件下很好的兼容(Table 4)。
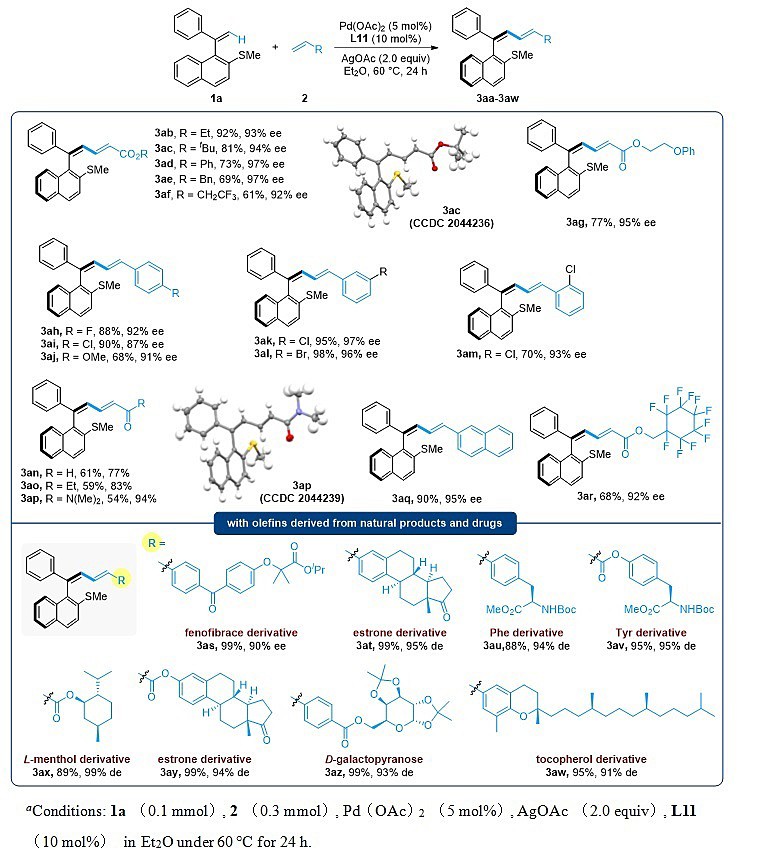
Table 4. Scope of Olefins. α
研究人员还将此策略应用于同时构建具有多个手性轴的手性苯乙烯(Table 5)。反应能以中等及以上的产率和优秀的对映选择性和非对映选择性得到目标的双轴手性苯乙烯产物。
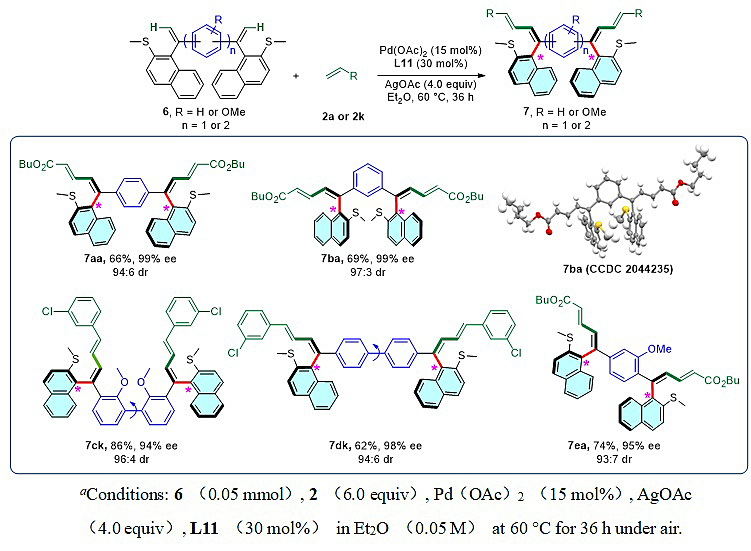
Table 5. Scope of Diaxially Chiral Styrenes α
为了考察该策略的合成应用前景,研究人员对反应进行了克级规模的放大和一系列的后续衍生化反应(Scheme 2)。
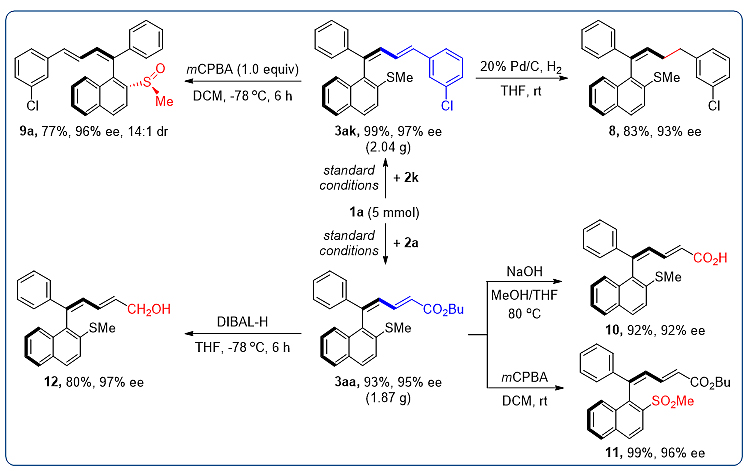
Scheme 2. Scale-Up Preparation and Derivatizations, and application.
最后研究人员将衍生化得到的轴手性烯烃亚砜化合物(9a-9e),作为一类新型的拥有手性轴结构的硫烯配体作用于铑催化的不对称共轭加成反应中。反应可以以优秀的产率和可观的对映选择性得到相对应的加成产物(Scheme 3)。
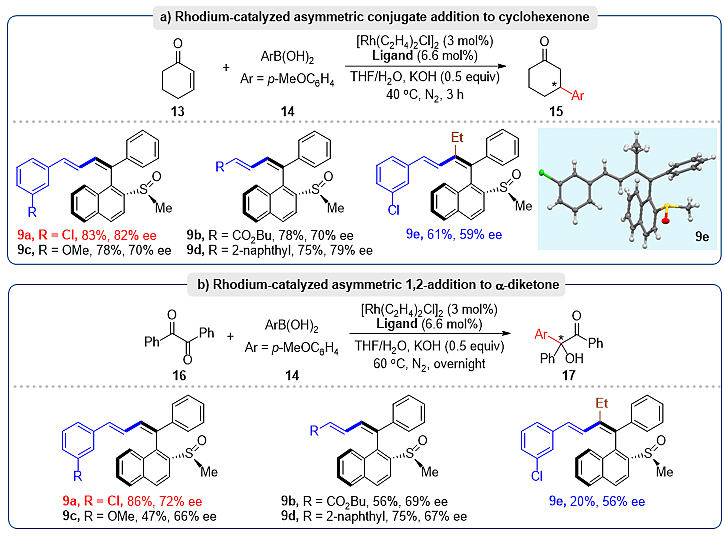
Scheme 3. Applications as a New Type of Chiral S-Olefin Ligands
总结
浙江大学史炳锋课题组报道了以Pd(II)催化不对称烯烃碳氢键烯基化策略构建具有多取代共轭二烯结构的手性苯乙烯化合物。该方法以硫醚作为导向基,不但可以取得优秀的产率(up to 99% yield)和对映选择性(up to 99% ee),以及完全的顺式选择性,而且可以合成一类具有手性轴结构的硫烯配体,在铑催化不对称加成反应中拥有潜在的应用前景。这一成果近期发表在Journal of the American Chemical Society 上,文章第一作者是浙江大学化学系博士研究生金良。浙江大学史炳锋教授为本文的通讯作者。
原文:Atroposelective Synthesis of Conjugated Diene-Based Axially Chiral Styrenes via Pd(II)-Catalyzed Thioether-Directed Alkenyl C–H Olefination. Liang Jin, Peng Zhang, Ya Li, Xin Yu, and Bing-Feng Shi* . J. Am. Chem. Soc., 2021, 143, 12335–12344, DOI: 10.1021/jacs.1c06236
史炳锋课题组链接http://mypage.zju.edu.cn/bfshi

