吴起课题组:【酶催化】光脱羧酶催化外消旋羧酸的选择性脱羧反应
带有α-官能团的手性羧酸是很多药物和天然产物的重要中间体或者结构砌块。目前已经有很多制备含α-官能团的手性羧酸的合成方法。通常的化学合成法需要用到过渡金属催化剂和复杂的手性配体。与化学法相比,生物催化可以以更加绿色和可持续的方式制备这一类重要的手性化合物。例如酮还原酶和亚胺还原酶都已经成功地用于从α-酮酸到α-羟基/氨基酸的转化,此外水解酶催化的酯或者酸的动力学拆分也是广泛使用的方法。然而这些生物催化方法通常需要辅因子的参与或者将酸提前制备为相应的酯或酰胺化合物。因而探索更加简单高效且不需辅因子的新型生物催化方法制备含α-官能团的手性羧酸显得极为重要。
化学系的吴起课题组最近报道了一种利用光脱羧酶来高效拆分含α-官能团的外消旋羧酸的新方法。他们选择了一种来源于小球藻(Chlorella variabilis)NC64A的脂肪酸光脱羧酶(CvFAP)作为催化剂,以2-羟基辛酸的脱羧反应为模型开展研究。CvFAP可将不同链长(C12-C22)的脂肪酸在无任何辅助因子的作用下脱羧生成相应的烷烃或者烯烃。他们设想CvFAP的催化空腔可能对外消旋酸具有立体选择性,从而可以利用脱羧反应来实现外消旋羧酸的手性拆分。然而,研究发现野生型CvFAP的催化活性较差,12小时光照反应后只有20%的底物转化率,底物的对映体过量值(ee)只有22%。为了解决该问题,他们对CvFAP进行了蛋白质工程化改造。
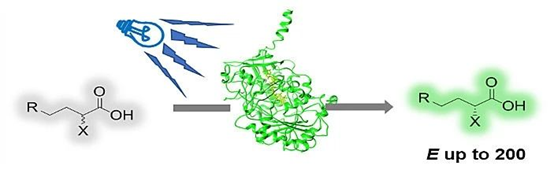
图1. 基于CvFAP酶进行含α-官能团的羧酸的光驱动动力学拆分。图片来源:Angew. Chem. Int. Ed.
定向进化中无论是随机突变还是饱和突变,突变株筛选的工作量都非常庞大。因此,他们在文章中采用了基于“大氨基酸扫描”策略的理性设计方法,结合CvFAP酶的晶体结构,选择了A384、L386和G462三个位点,将原有位点的氨基酸通过定点突变替换为包括Q、K、F和Y在内的大体积氨基酸。筛选结果发现突变株G462Y最好,可以在51%的转化率下获得99%ee值的R-构型底物。动力学测试结果表明G462Y突变株的活性相比野生型提高了30倍。进一步研究发现G462Y突变株具有较广泛的底物谱,一系列具有C6-C12不同链长或者具有不同取代基的α-羟基酸、以及α-氨基酸都能获得良好的手性拆分结果。分子动力学模拟发现在C462Y突变株中,活性位点周围的一些氨基酸有助于稳定R-构型底物,阻止它靠近FAD辅因子;而S-构型底物则与FAD中的N5原子具有更小的距离,从而使得S-构型羧酸底物更容易发生脱羧反应。
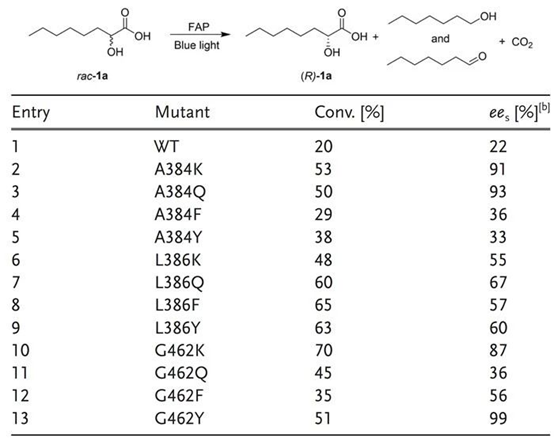
表1. 在选择位点引入大体积氨基酸(Q、K、F和Y)的效果评估。图片来源:Angew. Chem. Int. Ed.
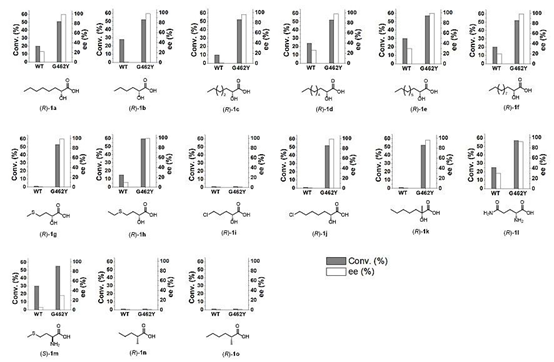
图2. 野生型CvFAP和C462Y突变体的光驱动动力学拆分的底物范围。图片来源:Angew. Chem. Int. Ed.
该研究第一次实现了光脱羧酶CvFAP的立体选择性脱羧反应,为手性羧酸的合成提供了一种新的方法,有望在制药、绿色有机合成等领域中获得重要的应用。
这一成果近日发表在Angew. Chem. Int. Ed.上。该文章的第一作者是化学系的博士生徐鉴,通讯作者为吴起副教授。
Light�Driven Kinetic Resolution of α�Functionalized Carboxylic Acids Enabled by an Engineered Fatty Acid Photodecarboxylase
Jian Xu, Yujing Hu, Jiajie Fan, Mamatjan Arkin, Danyang Li, Yongzhen Peng, Weihua Xu, Xianfu Lin, Qi Wu
Angew. Chem. Int. Ed., 2019, 58, 8474-8478, DOI: 10.1002/anie.201903165
科研思路分析
Q:这项研究最初是什么目的?或者说想法是怎么产生的?
A:我们课题组的研究兴趣是探索各种酶催化的新功能,以实现生物催化在有机合成领域中更广泛的应用。光脱羧酶CvFAP是法国Beisson教授和合作者于2017年最早发现并报道的一个能利用光能的酶(Science, 2017, 357, 903�907)。该酶催化的天然底物都是一些长链的脂肪酸,产物是一些没有手性中心的烷烃或者烯烃。酶作为一类具有高度立体选择性的催化剂,其手性空腔可以通过定向进化等蛋白质工程手段进行调节。因此,我们设想CvFAP脱羧酶的催化中心也应该是具有立体选择性的特质,如果底物是外消旋羧酸的话,很可能会导致两种构型羧酸的脱羧反应的活性区别,从而实现羧酸的高效拆分。而这样的酶催化拆分反应是从来没有报道过的。
Q:研究过程中遇到哪些挑战?
A:正如文中所述,野生型CvFAP对这些外消旋羧酸的反应活性很弱,虽然对于某些底物野生型CvFAP也体现出了较高的立体选择性,但是由于产物是没有手性的,因此难以获得高光学纯度的α-取代羧酸化合物。因此,本项研究中最大的挑战是如何提高CvFAP酶的催化活性。虽然酶的定向进化研究已经有了很多的报道,但是我们团队在酶蛋白质工程的理性设计方面的经验积累起了至关重要的作用(J. Am. Chem. Soc., 2019,141(19): 7934-7945; Chem. Commun., 2019, 55, 2198-2201; Adv. Synth. Catal.,2019, 361, 126-134; ACS Catal., 2017, 7, 4542−4549),可以让我们在少量突变株筛选的基础上就可以获得我们所需要的目标突变株。
Q:该研究成果可能有哪些重要的应用?哪些领域的企业或研究机构可能从该成果中获得帮助?
A:带有α-官能团的手性羧酸是很多药物和天然产物的重要中间体或者结构砌块。正如文中所述,我们发展的光脱羧酶催化外消旋羧酸的立体选择性拆分方法,和以前所报道的化学法、酶还原法或者水解酶催化拆分方法相比,具有一些独特的优势,例如光引发、不需要辅酶循环、以及酸底物的衍生化等。我们相信这项研究为手性羧酸的合成提供了一种新的方法,有望在制药、绿色有机合成等领域中获得重要的应用。
来源:X-MOL微信公众号

