丁寒锋课题组在天然产物全合成方面取得突破
来源:浙江大学化学系
发布时间:2013-11-04
17115
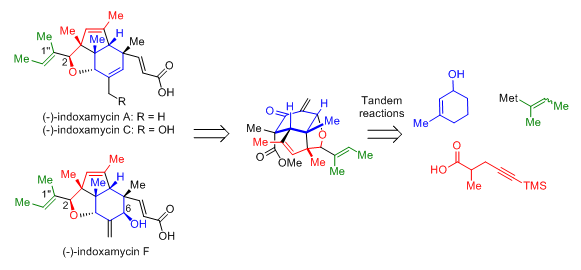
革兰氏阳性的放线菌科微生物已成为富含生物活性化合物的来源,其产生的微生物抗生素超过目前所有已发现抗生素的一半。过去五十年中,研究人员将主要目光聚集于陆地来源的细菌,并致力于从中发现活性小分子。最近,海洋微生物引起了很大重视,因为它们可以作为结构多样性天然产物的来源。2009年,日本的Sato小组从盐水养殖的海洋放线菌微生物中分离得到了一类新的聚酮结构,并将其命名为indoxamycins A‒F。在此家族中,indoxamycins A和F显示出对HT-29(人结肠癌)肿瘤细胞株显著的抑制生长活性(IC50相应为0.59 μM和0.31 μM),达到与传统化疗药物mitomycin相当的水平(IC50为0.66 μM)。从结构上看,此类分子独特的[5,6,6]三环骨架高度拥挤,分子内含有6个连续的手性中心(三个季碳中心,其中两个相邻),在全合成上具有极大的挑战性,已成为近年来化学合成的热门天然产物。
最近,丁寒锋课题组基于发散性策略,运用Ireland‒Claisen重排以及本组独立发展出的不对称还原烯炔环合反应和格式试剂促进的1,2-加成/氧杂Micheal/亚甲基化串联反应为关键步骤,从一个含有天然产物三环骨架结构的共同中间体(common intermediate)出发,分别实现了indoxamycin家族中分子A,C和F的首次全合成,并通过一系列中间体的单晶结构毫无争议地确定了其真实构型。该研究成果目前已发表在德国应用化学杂志(Angew. Chem. Int. Ed)上(http://onlinelibrary.wiley.com/doi/10.1002/anie.201307426/abstract)。此路线简洁高效、灵活通用的特性使得合成其余家族成员分子和类似物以进行进一步的生物活性筛选成为可能,后续工作正在进行之中。
该论文共同第一作者为2012级直博生何驰和2012级硕士生朱辰龙。该项工作得到了浙江大学化学系特聘研究员启动基金、国家自然科学基金(21202144),中央高校基本科研业务费(2011QNA3010、2013QNA3021),浙江省自然科学基金(LQ12B02003)和教育部博士点新教师基金(20120101120087)的资助。